- Raptor Biphenylは内因性マトリックス干渉から分析対象化合物の確実な分離を可能にします。
- C18や他のフェニル系固定相では分離が困難な化合物の選択性が高まり、正確な結果が得られます。
- 3分の高速分析によってさらなるサンプルのスループットの向上が可能となります。
コルチゾールは、副腎にて多酵素によるカスケード反応によってコレステロールから合成されるステロイドホルモンです。それはヒトにおける主要なグルココルチコイドであり、そしてグルコース代謝および免疫応答の制御において重要な役割を果たしています。コルチゾールの下流代謝産物であるコルチゾンは、さまざまな副腎皮質障害、特に副腎皮質機能亢進症(クッシング症候群)の診断に役立つように、コルチゾールと同時に測定されます。尿中遊離コルチゾールおよびコルチゾンレベルは生理活性を示す血漿中の濃度と良い相関があり、重要なバイオマーカーです。LC-MS / MSは選択性が高く、イムノアッセイに基づく方法に影響を与える可能性のある、分析における干渉を排除するのに役立つため、これらの化合物に適したスクリーニング技術です。
コルチゾールとコルチゾンの構造的な類似性、および尿成分からのマトリックス効果の可能性により、正確な結果を得るためには適切なカラム選択性が重要です。ここで開発された尿中遊離コルチゾールとコルチゾンのLC-MS/MS分析では、高い選択性を有するRaptor Biphenylカラムを使用することによって両方の化合物が内因性マトリックス干渉から完全に分離されました。いくつかのマトリックス化合物はコルチゾールとアイソバリックであり、質量分析計によって判別することができないので、この場合はクロマトグラフィー分離が不可欠でした。Raptor Biphenylカラムとここに示す条件を使用して、3分の分析でベースライン分離が得られました。これにより、臨床診断のためのより正確な定量データを迅速に生成できます。
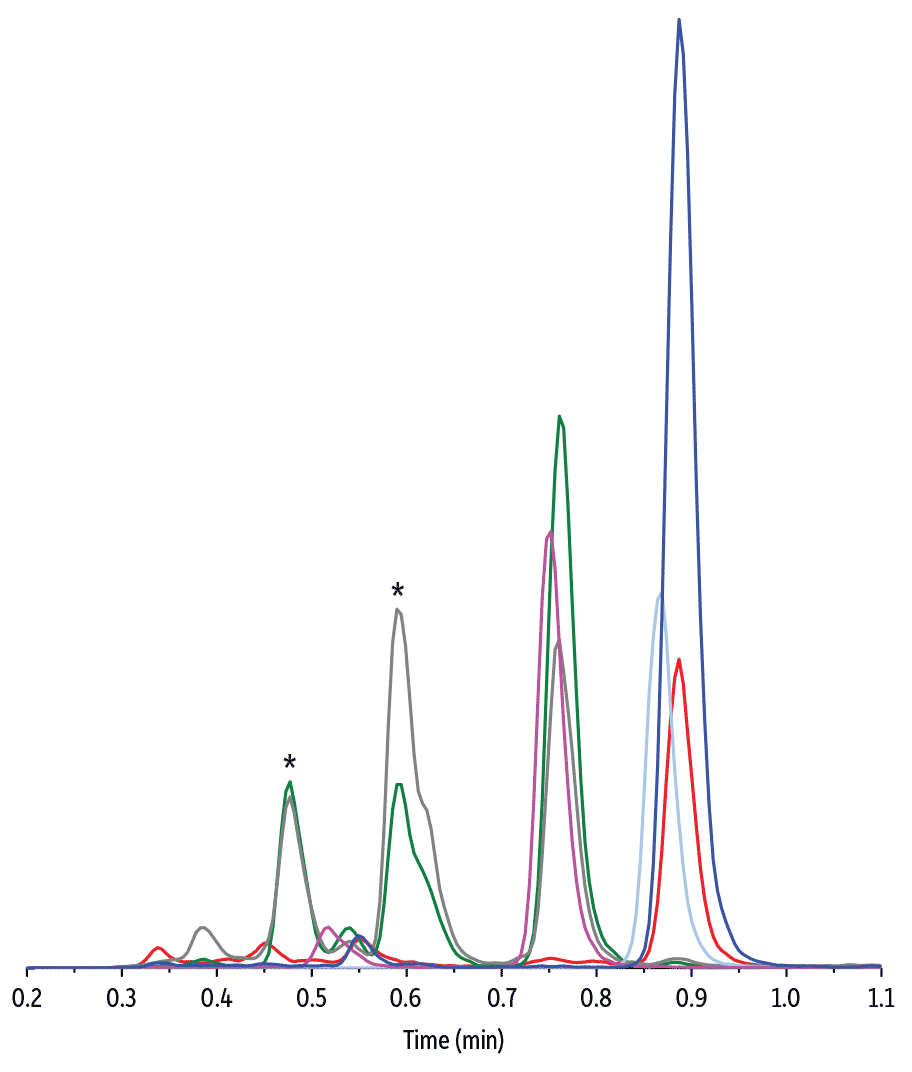
LC_CF0697
Peaks
| Peaks | tR (min) | Precursor Ion | Product Ion | Product Ion | |
|---|---|---|---|---|---|
| 1. | Cortisol-d4 | 0.75 | 367.4 | 121.0 | – |
| 2. | Endogenous cortisol | 0.76 | 363.3 | 120.9 | 91.1 |
| 3. | Cortisone-d8 | 0.88 | 369.4 | 167.9 | – |
| 4. | Endogenous cortisone | 0.89 | 361.3 | 163.2 | 91.0 |
Conditions
| Column | Raptor Biphenyl (cat.# 9309A52) | ||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Dimensions: | 50 mm x 2.1 mm ID | ||||||||||||||||||||||||||||
| Particle Size: | 2.7 µm | ||||||||||||||||||||||||||||
| Pore Size: | 90 Å | ||||||||||||||||||||||||||||
| Guard Column: | Raptor Biphenyl EXP guard column cartridge 5 mm, 2.1 mm ID, 2.7 µm (cat.# 9309A0252) | ||||||||||||||||||||||||||||
| Temp.: | 40 °C | ||||||||||||||||||||||||||||
| Standard/Sample | |||||||||||||||||||||||||||||
| Diluent: | Mobile phase A | ||||||||||||||||||||||||||||
| Conc.: | Calculated concentration is 105.1 ng/mL and 135.9 ng/mL for cortisol and cortisone, respectively | ||||||||||||||||||||||||||||
| Inj. Vol.: | 10 µL | ||||||||||||||||||||||||||||
| Mobile Phase | |||||||||||||||||||||||||||||
| A: | Water, 0.1% formic acid | ||||||||||||||||||||||||||||
| B: | Acetonitrile, 0.1% formic acid | ||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||
| Max Pressure: | 400 bar |
| Detector | MS/MS |
|---|---|
| Ion Mode: | ESI+ |
| Mode: | MRM |
| Instrument | UHPLC |
| Sample Preparation | 1. Centrifuge female human urine for 5 min at 4500 rpm, 10 °C. 2. Aliquot 380 µL supernatant. Add 20 µL each of internal standard solution (1 µg/mL in methanol). 3. Load 200 μL of sample on to ISOLUTE SLE+ 200 µL supported liquid extraction plate (part# 820-0200-P01). 4. Apply a pulse of vacuum to initiate flow. 5. Wait 5 min for sample to completely absorb. 6. Extract samples with 1 mL of MTBE. Allow solvent to flow for 5 min under gravity. Apply vacuum for 10-30 sec to complete elution. 7. Evaporate extracts to dryness under a stream of nitrogen. 8. Reconstitute in 200 µL mobile phase A prior to analysis. 9. Vortex to mix. |


