概要
飲料水および環境水(非飲料水)中の幅広いPFASモニタリングに関するニーズが高まる中、効率的な分析手法が求められています。本研究では、代替型(短鎖)および従来型(長鎖)PFASに加え、超短鎖PFASをターゲットとし、C2(超短鎖)を含む、C3、C4、C6、C8、および代替化合物の一斉分析手法を開発しました。以下に、実験の結果を報告します。
はじめに
超短鎖ペルおよびポリフルオロアルキル化合物(PFAS)は、分子サイズが小さく高極性であり、環境水中(雨、河川、地下水など)のPFAS総量の少なくとも40%を占めています [1, 2, 3]。超短鎖PFASには、トリフルオロ酢酸(TFA)、ペルフルオロプロパン酸(PFPrA)、ペルフルオロエタンスルホン酸(PFEtS)、およびペルフルオロプロパンスルホン酸(PFPrS)が含まれますが、最も環境中に多く存在するTFAは逆相(RP)カラムでの保持が不十分であるため、クロマトグラフィーによる分析が困難です。一方、陰イオン交換クロマトグラフィーを用いた分析方法では、超短鎖PFASは保持が強すぎるため、クロマトグラフィー性能が低下する傾向があります。そのため、超短鎖PFASを代替型PFASや従来型PFASと単一の分析メソッドを用いてモニタリングする場合、分析メソッドの開発はさらに難しい課題となります。
この課題を解決するため、Restekは独自のハイブリッドHILIC/イオン交換カラム(Raptor Polar X)を使用して、C2、C3、C4、C6、C8、および代替PFASを包括的に分析するための高速でシンプルなLC-MS/MSメソッドを開発しました。このカラムはバランスの取れたマルチモード(ミックスモード)保持機構を採用しているため、超短鎖PFASから長鎖PFASをイソクラティック条件で一斉に分析することが可能です。さらに、新たに開発した分析条件を用いて水道水、河川水、地下水、公的機関が運営する排水処理施設排水(POTW処理済み排水)を用いて添加サンプルを調製し、直接注入法にて分析を行ったところ、良好な再現性と精度が得られました。これらのことから、本分析法が、代替型および従来型PFASに加えて超短鎖PFASも含む幅広いPFAS成分を一斉に分析する上で有用であることが明らかとなりました。また、簡便な設定とハイスループットを求める水質検査ラボにとって、効率的かつ実用的な手法となることが示唆されました。
実験
分析メソッド:
分析条件は以下のとおりです。各分析対象成分に使用したトランジションと内部標準はTable Iに記載しています。
| カラム: | Raptor Polar X (2.7 µm, 50 mm x 2.1 mm ID [cat.# 9311A52]) | |
| カラム温度: | 40 °C | |
| 注入量: | 10 µL | |
| 移動相A: | 水、10 mMギ酸アンモニウム, 0.05%ギ酸 | |
| 移動相B: | アセトニトリル:メタノール (60:40), 0.05%ギ酸 | |
| グラジエント: | 時間(分) | %B |
| 0.00 | 85 | |
| 8.00 | 85 | |
| 流速: | 0.5 mL/min | |
| イオン化モード: | Negative ESI | |
| モード: | MRM | |
Table I: 水質サンプル中の代替型PFASおよび従来型PFAS、超短鎖PFASの分析対象成分MSトランジション
| 分析対象成分 | プレカーサイオン | プロダクトイオン | 定量用IS |
|---|---|---|---|
| TFA | 113.03 | 69.01 | 13C2-PFHxA |
| PFPrA | 163.03 | 119.01 | 13C2-PFHxA |
| PFBA | 212.97 | 168.97 | 13C2-PFHxA |
| PFHxA | 312.97 | 268.90 | 13C2-PFHxA |
| PFOA | 412.90 | 368.91 | 13C2-PFOA |
| HFPO-DA | 284.97 | 168.92 | 13C2-PFOA |
| ADONA | 376.90 | 250.93 | 13C2-PFOA |
| PFEtS | 198.98 | 79.92 | 13C3-PFBS |
| PFPrS | 248.97 | 79.98 | 13C3-PFBS |
| PFBS | 298.97 | 79.97 | 13C3-PFBS |
| PFHxS | 398.90 | 79.97 | 13C3-PFBS |
| PFOS | 498.84 | 79.97 | 13C4-PFOS |
| 9Cl-PF3ONS | 530.78 | 350.85 | 13C4-PFOS |
| 11Cl-PF3OUdS | 630.78 | 450.80 | 13C4-PFOS |
| 13C2-PFHxA | 314.97 | 269.93 | – |
| 13C2-PFOA | 414.90 | 369.87 | – |
| 13C3-PFBS | 301.90 | 79.97 | – |
| 13C4-PFOS | 502.84 | 79.97 | – |
サンプル前処理
ポリプロピレン製バイアル(バックグラウンド汚染を軽減するために使用)に、各水質サンプル250 µLにメタノール250 µLおよび内部標準溶液5 µL(メタノール中の13C2-PFHxA、13C2-PFOA、13C3-PFBS、13C4-PFOSの10 ng/mL)を加えて混合しました。このバイアルはバックグラウンド汚染をさらに軽減するため、ポリエチレン製キャップで密閉し、分析に使用しました。
校正用標準溶液は、脱イオン水(Thermo Scientific Barnstead E-Pureシステムで生成)を使用し、10~800 ng/Lの範囲で14種類の分析対象成分を添加して調製しました。これらの校正用標準溶液は、上記のサンプル前処理手順と同様に、メタノールで1:1に希釈しました。
Restek施設で採取した水道水サンプルと、米国環境保護庁(U.S. EPA)から提供された3種類の水質サンプル(シカゴの河川水、地下水、POTW処理済み排水)には、40pptと160pptの既知濃度となるよう成分を加え、水質添加サンプルとしました。ブランク水質サンプルおよび添加水質サンプルも、上記と同様にメタノールで1:1に希釈して分析を行い、校正用標準溶液を用いて定量しました。なお、地下水中のTFA濃度が高いことが明らかとなったため、この試料については脱イオン水で5倍に希釈した後、40pptおよび160pptとなるよう水質添加サンプルを調製しました。
結果と考察
分析条件について
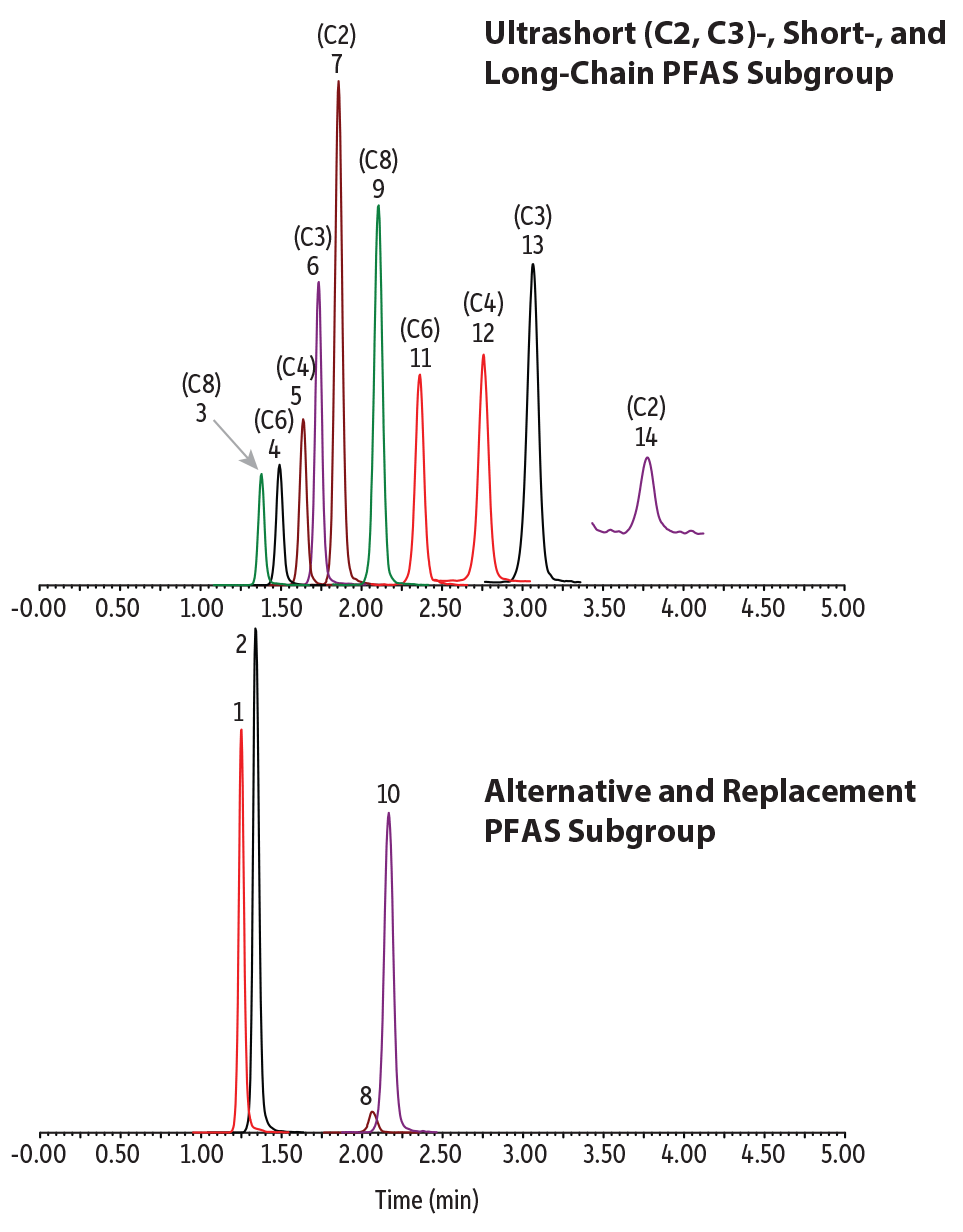
水質サンプル中の代替型PFASおよび従来型PFASともに、高速でシンプルな超短鎖PFAS分析を可能にするイソクラティック条件が確立されました。すべての分析対象成分は4分で溶出し、バランスのいい保持と良好なピーク形状を示しました(Figure 1)。サイクルタイムを8分間とすることで水質サンプルのいずれでもマトリックス干渉は観察されませんでした。後述するように、マトリックス干渉の可能性を回避するためには、最終溶出化合物の後に約4分間のホールドが必要であることが明らかとなりました。
直線性
TFAが20~800 ppt、他のすべての分析対象成が10~800 pptの範囲で検量線を作成しました。それぞれの分析対象成分に対して最適な標準曲線を決定するため、4種類の内部標準を評価しました。その結果、すべての成分において、1/x重み付け二次回帰を用いた場合において、r2値が0.996を超える良好な直線性を示し、偏差は20%未満であることが確認されました。
精度と再現性
最初の実験では、5分間のイソクラティック条件で水質サンプルの分析を行ったところ、TFAシグナルにマトリックス干渉が観察されました。そこで、分析時間について再検討した結果、すべての分析対象成分におけるマトリックス干渉を回避するためには、8分の分析時間が必要であることが判明しました。ただし、イソクラティックのホールド時間については、使用する装置および/または分析するサンプルによって変更する必要がある点に注意してください。
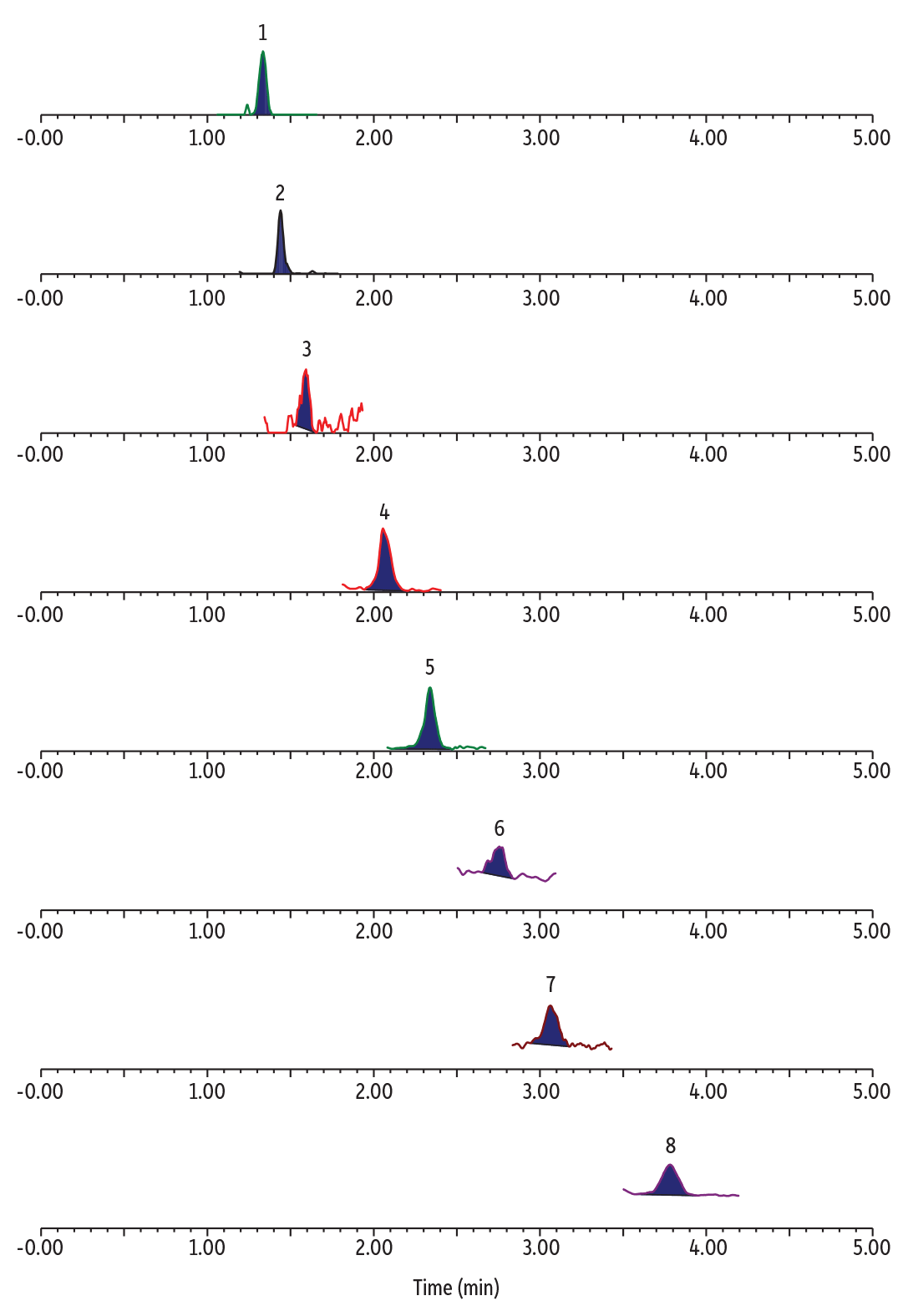
ブランク水質サンプルから、ADONA、HFPO-DA、9Cl-PF3ONS、11Cl-PF3OUdSは検出されませんでしたが、さまざまなレベルのTFA、C3、C4、C6、C8 PFASが検出されました(Table II)。POTWブランクサンプル中の代替型PFASおよび従来型PFAS、超短鎖PFASの一斉分析クロマトグラムを例としてFigure 2に示します。
Table II: ブランク水質サンプル中の検出可能な分析対象成分
| 検出濃度 (ng/L) | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| サンプル | TFA | PFPrA | PFBA | PFHxA | PFOA | HFPO-DA | ADONA | PFEtS | PFPrS | PFBS | PFHxS | PFOS | 9Cl-PF3ONS | 11Cl-PF3OUdS |
| 水道水 | 164.2 | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND |
| 河川水 | 193.3 | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND |
| 地下水 | 1425 | ND | ND | ND | 5.4 | ND | ND | ND | ND | 6.7 | 3.9 | ND | ND | ND |
| POTW水 | 352.8 | 9.6 | 15.3 | 93.5 | 20.4 | ND | ND | ND | ND | 6.8 | 6.7 | 9.6 | ND | ND |
ND: 不検出
精度の確認(回収率)では、ブランクサンプル中PFASの濃度を考慮し、添加サンプル中PFASの測定値を補正しました。水質サンプルは、低濃度および高濃度、それぞれn=2でサンプルを作成し、分析バッチごとに測定を行いました。合計3つの分析バッチを異なる日付で測定し、それぞれのデータを集計して精度と再現性を算出しました(Table III)。本手法の精度は、水質サンプル中の添加サンプルおよびLLOQ(定量下限)レベルの両方において、回収値が公称濃度の30%以内であることが示されました。また、%RSDが20%未満であったことから、本手法は、水中の超短鎖PFASを代替型および従来型PFASと同時に分析する場合においても、許容範囲の再現性が得られることが明らかとなりました。
Table III: メソッドの精度と再現性
| 平均%精度 (%RSD) | |||||||||
| マトリックス | 水道水 | 河川水 | 地下水** | POTW水 | 脱イオン水 | ||||
| 濃度 (ng/L) | 40 | 160 | 40 | 160 | 40 | 160 | 40 | 160 | 10* (LLOQ) |
| TFA | 106 (16.9) | 97.9 (7.10) | 97.4 (10.8) | 97.6 (6.12) | 97.5 (14.5) | 103 (8.87) | 102 (17.1) | 96.4 (7.33) | 107 (3.55) |
| PFPrA | 95.1 (4.08) | 105 (3.48) | 94.5 (6.85) | 104 (2.36) | 103 (9.37) | 105 (8.34) | 91.8 (4.90) | 104 (7.09) | 109 (1.61) |
| PFBA | 106 (6.80) | 117 (3.18) | 105 (7.40) | 114 (4.91) | 111 (2.48) | 120 (3.27) | 106 (6.58) | 114 (4.85) | 104 (4.91) |
| PFHxA | 93.3 (7.41) | 111 (2.61) | 91.8 (11.34) | 103 (4.55) | 102 (6.62) | 109 (7.11) | 103 (8.37) | 108 (3.13) | 115 (1.64) |
| PFOA | 100 (4.24) | 107 (3.14) | 103 (6.71) | 105 (2.64) | 92.6 (3.85) | 107 (3.09) | 102 (4.57) | 109 (3.64) | 106 (3.28) |
| HFPO-DA | 95.7 (11.9) | 108 (9.05) | 86.6 (8.97) | 104 (5.45) | 94.1 (18.6) | 105 (9.35) | 95.2 (8.49) | 106 (9.23) | 102 (16.8) |
| ADONA | 106 (3.75) | 116 (2.38) | 100 (6.86) | 110 (4.59) | 104 (4.91) | 113 (5.23) | 111 (5.26) | 115 (2.65) | 105 (4.76) |
| PFEtS | 94.8 (9.68) | 110 (5.39) | 89.4 (7.43) | 102 (9.76) | 96.5 (4.09) | 108 (6.11) | 104 (8.18) | 109 (5.23) | 99.8 (9.85) |
| PFPrS | 104 (4.97) | 115 (4.19) | 95.0 (3.87) | 107 (4.26) | 106 (10.6) | 114 (3.36) | 111 (4.88) | 114 (2.96) | 108 (3.28) |
| PFBS | 97.4 (10.1) | 113 (3.97) | 93.6 (5.24) | 104 (4.19) | 97.8 (4.47) | 107 (4.23) | 94.1 (10.7) | 108 (4.48) | 100 (11.0) |
| PFHxS | 99.4 (15.7) | 114 (3.56) | 94.3 (9.79) | 104 (5.28) | 95.2 (5.63) | 112 (3.20) | 104 (8.19) | 111 (4.07) | 107 (11.7) |
| PFOS | 104 (7.54) | 107 (7.69) | 103 (8.43) | 105 (7.23) | 97.3 (14.9) | 110 (4.84) | 109 (7.47) | 108 (7.53) | 102 (4.20) |
| 9Cl-PF3ONS | 98.7 (3.52) | 105 (8.35) | 91.8 (7.66) | 103 (5.68) | 94.7 (9.83) | 105 (8.90) | 105 (6.76) | 107 (8.27) | 107 (4.31) |
| 11Cl-PF3OUdS | 106 (10.1) | 113 (3.54) | 95.0 (3.52) | 113 (8.15) | 107 (6.61) | 112 (4.54) | 119 (4.25) | 120 (9.10) | 98.2 (11.3) |
*TFAのLLOQは20 ng/L
**TFAに関してのみ地下水を5倍希釈
結論
以上のことから、本研究で開発した手法は、飲料水や環境水(非飲料水)中でターゲットとなる従来のPFAS測定に加え、C2およびC3化合物を含む幅広いPFASを効率的に分析する上で、有効であることが示されました。この結果、PFAS一斉分析のメソッドとして信頼性が高く、分析ラボにおいて重要な手法となる可能性が示唆されました。
PFAS分析に関するさらなる情報は、www.restek.com/PFAS-JPから確認できます!
参考文献
- S. Taniyasu, K. Kannan, L.W.Y. Yeung, K.Y. Kwok, P.K.S Lam, N. Yamashita, Analysis of trifluoroacetic acid and other short-chain perfluorinated acids (C2-C4) in precipitation by liquid chromatography-tandem mass spectrometry: comparison to patterns of long-chain perfluorinated acids (C5-C18), Anal. Chim. Acta. 619 (2008) 221-230. https://pubmed.ncbi.nlm.nih.gov/18558116/
- J. Janda, K. Nodler, H-J. Brauch, C. Zwiener, F.T. Lange, Robust trace analysis of polar (C2-C8) perfluorinated carboxylic acids by liquid chromatography-tandem mass spectrometry: method development and application to surface water, groundwater, and drinking water, Environ. Sci. Pollut.R. 26 (2018) 7326-7336. https://pubmed.ncbi.nlm.nih.gov/29557039/
- K.Y. Kwok, S. Taniyasu, L.W.Y. Yeung, M.B. Murphy, P.K.S. Lam, Y. Horii, K. Kannan, G. Petrick, R.K. Sinha, N. Yamashita, Flux of perfluorinated chemicals through wet deposition in Japan, the United States, and other countries, Environ. Sci. Technol. 44 (2010) 7043-7049. https://pubmed.ncbi.nlm.nih.gov/20795671/