Élements clés
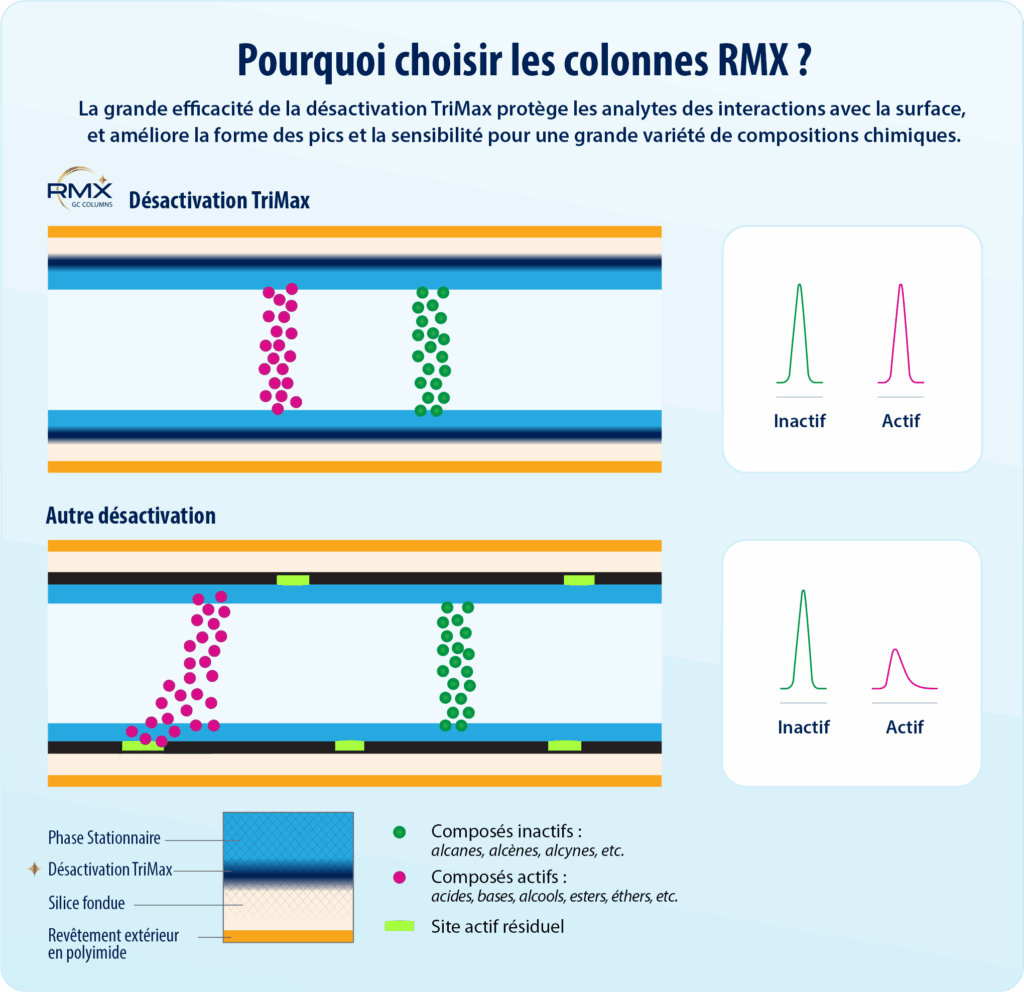
- La désactivation ultra efficace des colonnes GC produit un circuit d’échantillon exceptionnellement inerte.
- L’inertie maximale permet d’obtenir des pics fins et symétriques et des limites de détection instrumentalesinstrumentales (IDL) ≤ 10pg pour une large gamme de composés semi-volatils difficiles à analyser.
- Les objectifs de qualité des données pour les courbes l’étalonnage ont été facilement atteints. Pour l’ensemble des composés semi-volatils, l’écart-type relatif est ≤ 20 %, et les points d’étalonnage les plus bas étaient compris entre 1 et 10 ppb pour tous les composés, sauf pour l’acide benzoïque (50 ppb).


Résumé
Cette note d’application évalue les performances de la colonne RMX-5Sil MS pour l’analyse en GC-MS/MS des composés organiques semi-volatils à l’état de traces. Des limites de détection instrumentales de 10 picogrammes, voire moins, ont été atteintes pour tous les composés, à l’exception de l’acide benzoïque (14,70 pg) et du 2,4-dinitrophénol (11,53 pg).
L’écart-type relatif (%RSE) des courbes d’étalonnage était ≤ 20 % pour tous les composés. Les gammes d’étalonnage allaient de 1-1000 ppb à 10-1000 ppb pour tous les composés hormis l’acide benzoïque dont la plage s’étendait de 50 à 1000 ppb.
Introduction
Les laboratoires environnementaux analysent régulièrement les composés organiques semi-volatils (COSV) par GC-MS ou par GC-MS/MS, comme la méthode EPA US 8270E par exemple. Les laboratoires adoptent de plus en plus les méthodes GC-MS/MS car la meilleure sélectivité du détecteur permet des analyses plus sensibles telles que celles requises pour la méthode de micro-extraction EPA 3511. Cette méthode permet un gain de temps et une réduction de la consommation de solvant par rapport aux méthodes classiques de préparation des échantillons, pouvant utiliser jusqu’à un litre d’échantillon. Pour profiter pleinement de la sensibilité de la MS/MS, la colonne analytique doit présenter une haute inertie afin d’optimiser le rapport signal/bruit.
Une désactivation efficace de la colonne est essentielle pour garantir de bonnes performances de la méthode sur une large gamme de compositions chimiques, qui interagissent par divers mécanismes avec les sites actifs présents à la surface de la colonne. Dans cette étude, la colonne RMX-5Sil MS a été évaluée de manière indépendante sur ses performances analytiques pour une large gamme de composés semi-volatils à l’état de traces, notamment pour des composés connus difficiles à analyser. Les performances analytiques et les plages d’étalonnage ont été étudiées pour évaluer la capacité de la colonne à atteindre des niveaux de détection de l’ordre de picogramme.
Méthode expérimentale
Préparation des étalons
Des solutions d’étalonnage multi-composés ont été préparés dans le chlorure de méthylène à partir des solutions étalons commercialisées, sur une gamme de concentration de 1 à 1000 ppb (11 points).
Conditions analytiques
Les échantillons ont été analysés sur une colonne RMX-5Sil MS de 30 m, DI 0.25 mm, 0.25 μm (réf. 17323). Un GC Shimadzu Nexis GC-2030 couplé à un spectromètre de masse triple-quad Shimadzu “GCMS-TQ8050 NX” équipé d’une source IE et d’une cellule de collision UFsweeper de hautes performances a été utilisé pour l’analyse des composés semi-volatils par GC-MS/MS, selon les conditions ci-dessous.
Tableau I : Conditions de la méthode d’analyse des traces de composés semi-volatils par GC-MS/MS
| Chromatographe en phase gazeuse | Shimadzu Nexis GC-2030 |
| Colonne | RMX-5Sil MS, 30 m x DI 0.25 mm x 0.25 µm (réf. 17323) |
| Mode d’écoulement | Vitesse linéaire constante (39,5 cm/s) |
| Mode d’injection | Split (5:1) |
| Insert d’injection | Insert Topaz Gooseneck, DI 3,5 mm avec laine de quartz (réf. 23336) |
| Volume d’injection | 1 µl |
| Température de l’injecteur | 275 °C |
| Programmation du four | 40 °C (maintien 1,5 min) à 280 °C à 20 °C/min, puis une rampe de 5 °C/min jusqu’à 320 °C (maintien 1 min) |
| Système MS | Spectromètre de masse ultra-rapide Shimadzu GCMS-TQ8050 NX équipé d’une source IE et d’une cellule de collision UFsweeper haute performance |
| Ionisation | Impact électronique |
| Énergie d’ionisation | 70 eV |
| Courant d’émission | 60 mA |
| Mode d’acquisition | MRM |
| Gaz de collision | Argon |
| Température de la source | 230 °C |
| Température de la ligne de transfert | 300 °C |
Résultats et discussion
Performances chromatographiques
Dans l’ensemble, la colonne RMX-5Sil MS a produit des formes de pics et des séparations excellentes pour 86 composés semi-volatils analysés à 50 ppb. L’élution du dernier composé a eu lieu en moins de 21 minutes (Figure 1). Pour évaluer l’inertie de la colonne, les trainées de pics ont été mesurées aux extrémités basse et haute de la plage d’étalonnage linéaire pour des composés acides et basiques réputés particulièrement complexes. La Figure 2 montre que la surface inerte a limité l’interaction des composés avec la surface à des faibles concentrations, et a amélioré la symétrie des pics. Elle a donc permis une intégration facile et précise, même pour les composés difficiles à intégrer à de faibles concentrations. En outre, la surface n’a pas altéré la sélectivité des polymères, comme le montre la bonne séparation de la paire d’hydrocarbures aromatiques polycycliques (HAP), à élution rapprochée, le benzo(b) fluoranthène et le benzo(k)fluoranthène, à une concentration de 1 ppb.
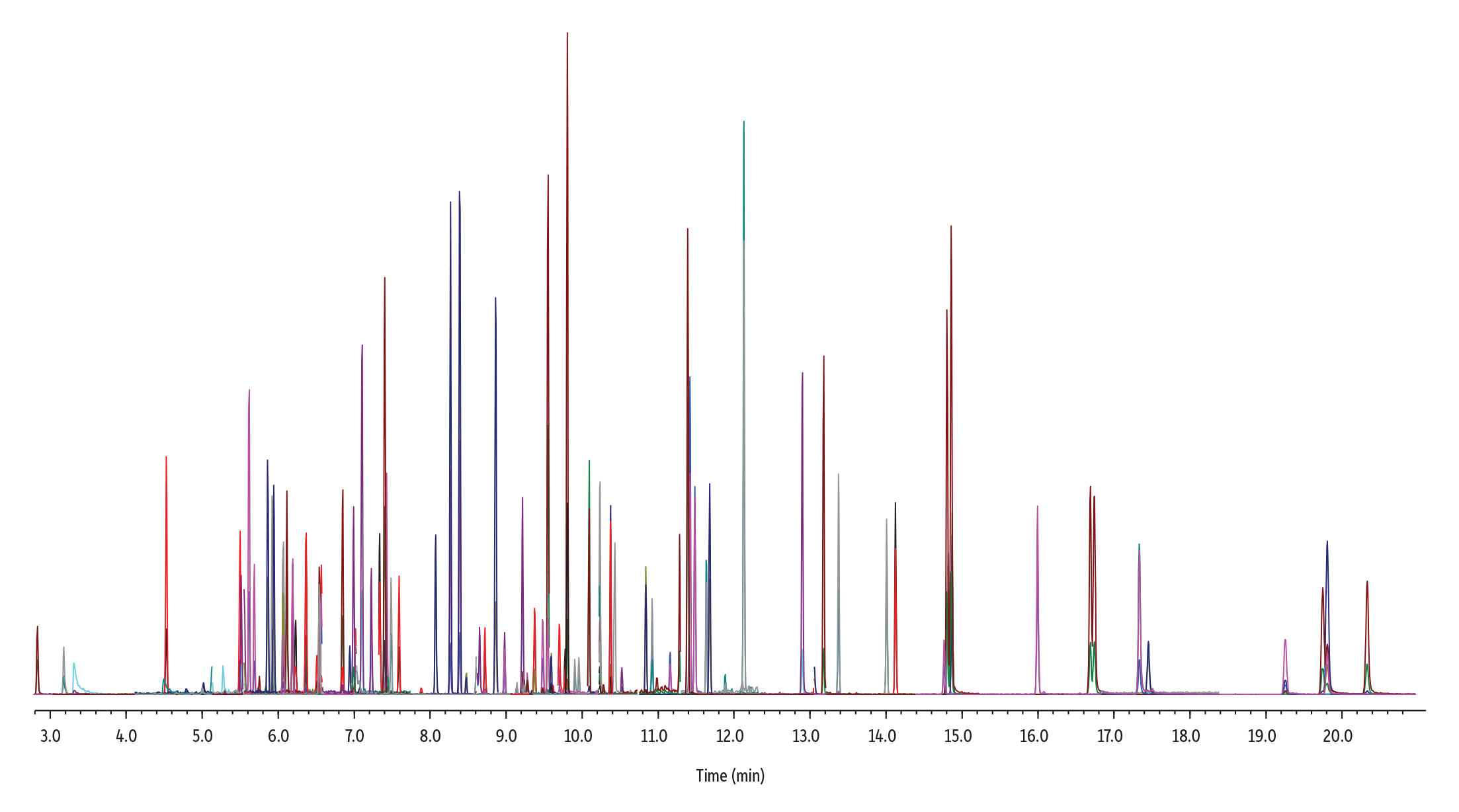
GC_EV1534
Peaks
| Peaks | tR (min) | Transition 1 | Collision energy 1 | Transition 2 | Collision energy 2 | |
|---|---|---|---|---|---|---|
| 1. | N-Nitrosodimethylamine | 3.173 | 74.00>44.10 | 6 | 74.00>42.10 | 18 |
| 2. | Pyridine | 3.276 | 79.10>50.10 | 21 | 79.10>52.10 | 15 |
| 3. | 2-Fluorophenol | 4.532 | 112.00>64.10 | 18 | 112.00>92.10 | 9 |
| 4. | Phenol | 5.514 | 94.00>66.00 | 9 | 66.00>40.00 | 12 |
| 5. | Phenol-d5 Surr | 5.5 | 99.00>71.10 | 12 | 99.00>69.10 | 27 |
| 6. | Aniline | 5.554 | 93.00>66.10 | 18 | 93.00>51.10 | 30 |
| 7. | Bis(2-chloroethyl) ether | 5.619 | 93.00>63.10 | 9 | 95.00>65.00 | 6 |
| 8. | 2-Chlorophenol | 5.688 | 128.00>64.00 | 18 | 128.00>91.90 | 15 |
| 9. | 1,3-Dichlorobenzene | 5.863 | 146.00>111.10 | 21 | 146.00>75.20 | 30 |
| 10. | 1,4-Dichlorobenzene | 5.944 | 146.00>111.10 | 21 | 146.00>75.20 | 30 |
| 11. | Benzyl alcohol | 6.069 | 79.00>77.10 | 12 | 107.00>79.10 | 9 |
| 12. | 1,2-Dichlorobenzene | 6.116 | 146.00>111.10 | 21 | 146.00>75.20 | 30 |
| 13. | 2-Methylphenol | 6.194 | 108.00>77.00 | 27 | 108.00>79.00 | 18 |
| 14. | 2,2′-oxybis(1-chloropropane) | 6.229 | 121.05>77.00 | 9 | 121.05>45.00 | 6 |
| 15. | 3 and 4-Methylphenol | 6.369 | 107.10>77.10 | 15 | 107.10>79.10 | 6 |
| 16. | N-Nitrosodi-N-propylamine | 6.374 | 130.10>113.10 | 4 | 130.10>88.10 | 4 |
| 17. | Hexachloroethane | 6.511 | 117.00>81.90 | 30 | 119.00>83.80 | 33 |
| 18. | Nitrobenzene | 6.563 | 77.05>51.00 | 21 | 123.05>77.00 | 15 |
| 19. | Nitrobenzene-d5 | 6.541 | 82.00>54.10 | 18 | 128.00>82.10 | 18 |
| 20. | Isophorone | 6.846 | 82.00>54.00 | 9 | 138.00>82.00 | 18 |
| 21. | 2-Nitrophenol | 6.941 | 139.00>109.10 | 9 | 139.00>81.00 | 12 |
| 22. | 2,4-Dimethylphenol | 6.99 | 107.00>77.10 | 18 | 122.00>107.10 | 18 |
| 23. | Benzoic Acid | 7.019 | 122.10>105.10 | 9 | 105.10>77.10 | 15 |
| 24. | Bis(2-chloroethoxy)methane | 7.102 | 93.00>63.10 | 9 | 95.00>65.00 | 6 |
| 25. | 2,4-Dichlorophenol | 7.223 | 162.00>63.10 | 33 | 164.00>63.10 | 30 |
| 26. | 1,2,4-Trichlorobenzene | 7.333 | 180.00>109.00 | 30 | 180.00>145.10 | 18 |
| 27. | Naphthalene | 7.424 | 128.10>102.10 | 20 | 128.10>78.00 | 20 |
| 28. | 2,6-Dichlorophenol | 7.223 | 136.00>108.10 | 27 | 136.00>134.10 | 27 |
| 29. | 4-Chloroaniline | 7.484 | 127.00>65.10 | 27 | 127.00>92.10 | 18 |
| 30. | Hexachlorobutadiene | 7.59 | 225.00>189.80 | 21 | 225.00>155.00 | 30 |
| 31. | 4-Chloro-3-methylphenol | 8.072 | 107.00>77.10 | 18 | 142.00>107.00 | 18 |
| 32. | 2-Methylnaphthalene | 8.268 | 142.10>115.10 | 28 | 115.10>89.00 | 16 |
| 33. | 1-Methylnaphthalene | 8.388 | 142.10>115.10 | 28 | 115.10>89.00 | 16 |
| 34. | Hexachlorocyclopentadiene | 8.474 | 237.00>141.00 | 27 | 237.00>143.00 | 27 |
| 35. | 2,4,6-Trichlorophenol | 8.613 | 196.00>97.00 | 33 | 198.00>97.00 | 30 |
| 36. | 2,4,5-Trichlorophenol | 8.651 | 196.00>97.00 | 33 | 198.00>97.00 | 30 |
| 37. | 2-Fluorobiphenyl | 8.721 | 172.00>151.20 | 27 | 172.00>146.10 | 27 |
| 38. | 2-Chloronaphthalene | 8.862 | 162.00>127.10 | 18 | 162.00>77.10 | 33 |
| 39. | 2-Nitroaniline | 8.979 | 138.00>92.00 | 15 | 138.00>65.10 | 33 |
| 40. | 1,4-Dinitrobenzene | 9.143 | 168.00>75.10 | 30 | 168.00>92.00 | 15 |
| 41. | Dimethylphthalate | 9.216 | 163.00>77.20 | 15 | 163.00>133.10 | 15 |
| 42. | 1,3-Dinitrobenzene | 9.14 | 168.00>75.00 | 30 | 168.00>122.00 | 12 |
| 43. | 2,6-Dinitrotoluene | 9.281 | 165.00>90.00 | 15 | 165.00>63.10 | 33 |
| 44. | Acenapthylene | 9.374 | 152.10>150.10 | 28 | 152.10>126.10 | 28 |
| 45. | 3-Nitroaniline | 9.484 | 92.05>65.00 | 12 | 138.05>65.00 | 27 |
| 46. | Acenaphthene | 9.592 | 152.10>150.10 | 28 | 152.10>126.10 | 28 |
| 47. | 2,4-Dinitrophenol | 9.617 | 184.05>107.00 | 12 | 154.05>107.00 | 6 |
| 48. | 4-Nitrophenol | 9.689 | 109.05>81.00 | 12 | 109.05>53.10 | 18 |
| 49. | 2,4-Dinitrotoluene | 9.778 | 89.05>63.10 | 18 | 165.05>119.00 | 6 |
| 50. | Dibenzofuran | 9.805 | 168.00>139.10 | 24 | 139.00>89.10 | 21 |
| 51. | 2,3,5,6-Tetrachlorophenol | 9.904 | 230.00>130.90 | 36 | 232.00>132.90 | 36 |
| 52. | 2,3,4,6-Tetrachlorophenol | 9.958 | 230.00>130.90 | 36 | 232.00>132.90 | 36 |
| 53. | Diethylphthalate | 10.093 | 149.00>65.00 | 30 | 177.00>149.10 | 12 |
| 54. | 4-Chlorophenyl phenyl ether | 10.234 | 141.00>115.20 | 21 | 204.00>141.20 | 21 |
| 55. | Fluorene | 10.23 | 165.10>163.10 | 28 | 165.10>115.10 | 28 |
| 56. | 4-Nitroaniline | 10.234 | 138.00>108.10 | 12 | 108.00>80.00 | 12 |
| 57. | 4,6-Dinitro-2-methylphenol | 10.283 | 198.05>121.00 | 12 | 198.05>53.00 | 27 |
| 58. | N-Nitrosodiphenylamine (Diphenylamine) | 10.376 | 169.00>167.20 | 27 | 168.00>139.00 | 39 |
| 59. | Diphenylhydrazine | 10.429 | 77.00>51.20 | 15 | 77.00>74.10 | 33 |
| 60. | 2,4,6-Tribromophenol | 10.524 | 329.80>141.00 | 36 | 331.80>142.90 | 36 |
| 61. | 4-Bromophenyl phenyl ether | 10.839 | 250.00>141.10 | 21 | 248.00>141.10 | 18 |
| 62. | Hexachlorobenzene | 10.922 | 283.80>248.80 | 24 | 283.80>213.80 | 28 |
| 63. | Pentachlorophenol | 11.159 | 265.90>164.90 | 26 | 265.90>166.90 | 26 |
| 64. | Phenanthrene | 11.421 | 178.10>176.10 | 28 | 178.10>152.10 | 20 |
| 65. | Anthracene | 11.484 | 178.10>176.10 | 28 | 178.10>152.10 | 20 |
| 66. | Carbazole | 11.68 | 167.00>139.20 | 27 | 166.00>140.00 | 18 |
| 67. | Di-n-butylphthalate | 12.131 | 149.00>93.10 | 18 | 149.00>65.10 | 24 |
| 68. | Fluoranthene | 12.9 | 202.10>200.10 | 30 | 200.10>198.10 | 30 |
| 69. | Benzidine | 13.062 | 184.00>156.10 | 24 | 184.00>167.10 | 24 |
| 70. | Pyrene | 13.18 | 202.10>200.10 | 30 | 200.10>198.10 | 30 |
| 71. | o-Terphenyl-D14 | 13.377 | 244.00>240.10 | 30 | 244.00>226.20 | 18 |
| 72. | Butylbenzylphthalate | 14.012 | 149.00>65.10 | 24 | 149.00>93.10 | 18 |
| 73. | Bis(2-ethylhexyl)adipate | 14.129 | 129.00>55.10 | 21 | 129.00>101.10 | 9 |
| 74. | 3’3-Dichlorobenzidine | 14.769 | 212.00>180.10 | 24 | 212.00>196.20 | 21 |
| 75. | Benz[a]anthracene | 14.805 | 228.10>226.10 | 32 | 226.10>224.10 | 32 |
| 76. | Bis(2-ethylhexyl)phthalate | 14.875 | 149.00>65.10 | 24 | 167.00>149.10 | 15 |
| 77. | Chrysene | 14.861 | 228.10>226.10 | 32 | 226.10>224.10 | 32 |
| 78. | Di-n-octylphthalate | 16 | 149.00>65.10 | 24 | 149.00>93.20 | 18 |
| 79. | Benzo[b]fluoranthene | 16.691 | 252.10>250.10 | 36 | 250.10>248.10 | 36 |
| 80. | Benzo[k]fluoranthene | 16.746 | 252.10>250.10 | 36 | 250.10>248.10 | 36 |
| 81. | Benzo[a]pyrene | 17.338 | 252.10>250.10 | 36 | 250.10>248.10 | 36 |
| 82. | Dibenz[a,j]acridine | 19.26 | 279.00>277.10 | 33 | 279.00>250.00 | 45 |
| 83. | Indeno[1,2,3-cd]pyrene | 19.754 | 276.10>274.10 | 36 | 274.10>272.10 | 36 |
| 84. | Dibenz[a,h]anthracene | 19.813 | 278.10>276.10 | 36 | 278.10>274.10 | 60 |
| 85. | Benzo[g,h,i]perylene | 20.339 | 276.10>274.10 | 36 | 274.10>272.10 | 36 |
Conditions
| Column | RMX-5Sil MS, 30 m, 0.25 mm ID, 0.25 µm (cat.# 17323) |
|---|---|
| Injection | |
| Inj. Vol.: | 1 µL split (split ratio 5:1) |
| Liner: | Topaz 3.5 mm ID single taper inlet liner w/wool (cat.# 23336) |
| Inj. Temp.: | 275 °C |
| Oven | |
| Oven Temp.: | 40 °C (hold 1.5 min) to 280 °C at 20 °C/min to 320 °C at 5 °C/min (hold 1 min) |
| Carrier Gas | He, constant flow |
| Linear Velocity: | 39.5 cm/sec @ 40 °C |
| Detector | SRM/MRM |
|---|---|
| Acquisition Type: | SRM/MRM |
| Source Temp.: | 230 °C |
| Transfer Line Temp.: | 300 °C |
| Analyzer Type: | Triple Quadrupole |
| Ionization Mode: | EI |
| Collision Gas: | Ar |
| Tune Type: | PFTBA |
| Tune Emission Current: | 60 μA |
| Notes | Shimadzu Nexis GC-2030 with Shimadzu GCMS-TQ8050 NX ultra-fast mass spectrometer with EI source and UFsweeper high-efficiency collision cell |
| Acknowledgement | Shimadzu |
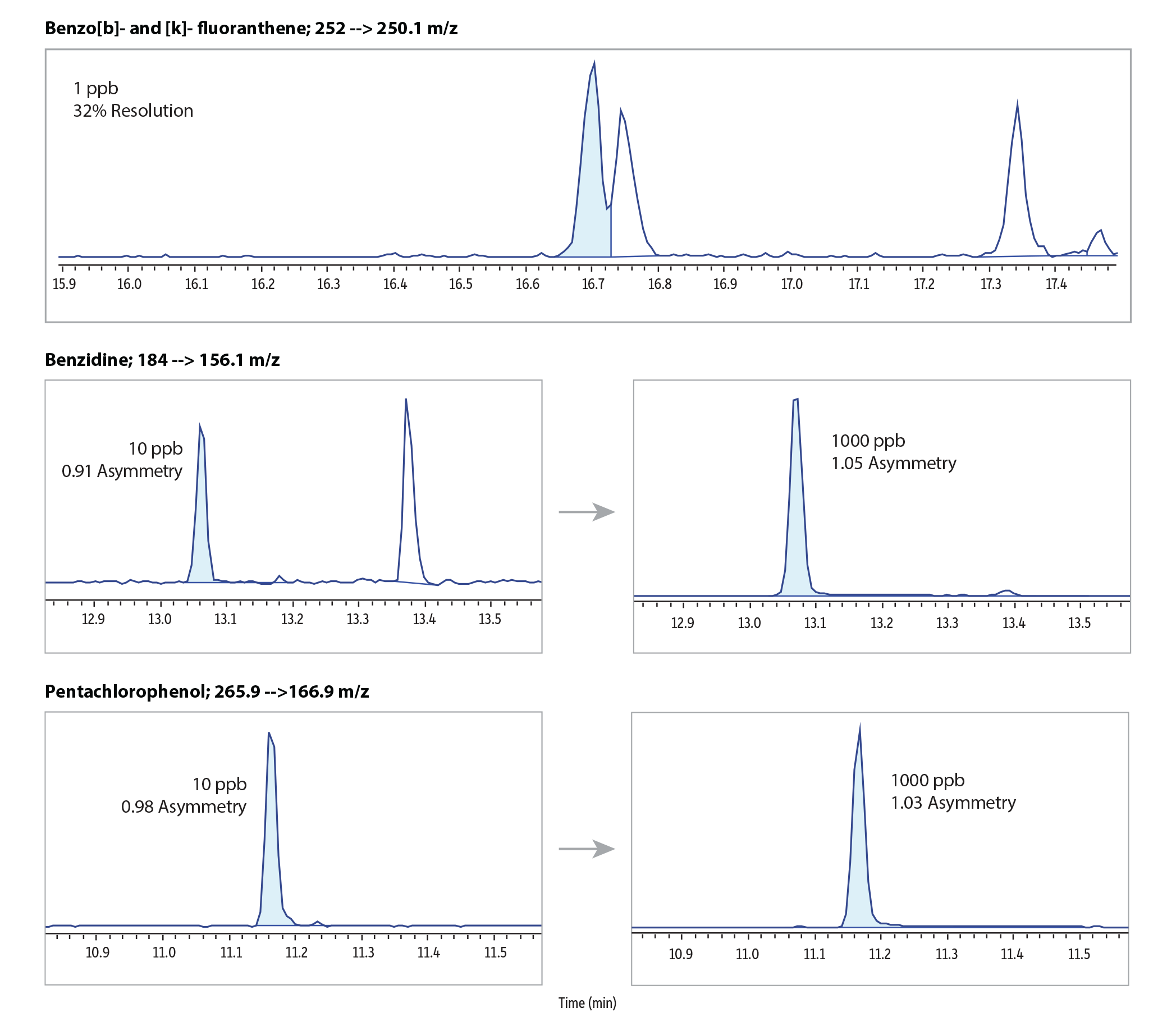
GC_EV1535
Peaks
| Peaks | tR (min) | Transition 1 | Collision energy 1 | Transition 2 | Collision energy 2 | |
|---|---|---|---|---|---|---|
| 1. | Benzidine | 13.062 | 184.00>156.10 | 24 | 184.00>167.10 | 24 |
| 2. | Benzo[b]fluoranthene | 16.691 | 252.10>250.10 | 36 | 250.10>248.10 | 36 |
| 3. | Benzo[k]fluoranthene | 16.746 | 252.10>250.10 | 36 | 250.10>248.10 | 36 |
| 4. | Pentachlorophenol | 11.159 | 265.90>164.90 | 26 | 265.90>166.90 | 26 |
Conditions
| Column | RMX-5Sil MS, 30 m, 0.25 mm ID, 0.25 µm (cat.# 17323) |
|---|---|
| Injection | |
| Inj. Vol.: | 1 µL split (split ratio 5:1) |
| Liner: | Topaz 3.5 mm ID single taper inlet liner w/wool (cat.# 23336) |
| Inj. Temp.: | 275 °C |
| Oven | |
| Oven Temp.: | 40 °C (hold 1.5 min) to 280 °C at 20 °C/min to 320 °C at 5 °C/min (hold 1 min) |
| Carrier Gas | He, constant flow |
| Linear Velocity: | 39.5 cm/sec @ 40 °C |
| Detector | SRM/MRM |
|---|---|
| Acquisition Type: | SRM/MRM |
| Source Temp.: | 230 °C |
| Transfer Line Temp.: | 300 °C |
| Analyzer Type: | Triple Quadrupole |
| Ionization Mode: | EI |
| Collision Gas: | Ar |
| Tune Type: | PFTBA |
| Tune Emission Current: | 60 μA |
| Notes | Shimadzu Nexis GC-2030 with Shimadzu GCMS-TQ8050 NX ultra-fast mass spectrometer with EI source and UFsweeper high-efficiency collision cell |
| Acknowledgement | Shimadzu |
Performances d’étalonnage
Le Tableau II montre que la combinaison du système GC-MS/MS Shimadzu avec la colonne RMX-5Sil MS ultra-inerte a permis d’atteindre une sensibilité exceptionnelle pour une grande variété de classes de composés semi-volatils à l’état de traces. L’écart-type relatif de la courbe d’étalonnage ≤ 20 % était conforme aux objectifs de qualité des données pour l’étalonnage. En outre, la valeur du R2, déterminée pour un sous-ensemble représentatif de composés semi-volatils, était ≥ 0,99 pour tous les composés évalués.
Pour la totalité des composés semi-volatils, les courbes d’étalonnage variaient de 1-1000 ppb à 10-1000 ppb, à part l’acide benzoïque (courbe d’étalonnage : 50-1000 ppb). Cette plage linéaire légèrement plus haute pour l’acide benzoïque était attendue, en raison de sa faible solubilité dans les phases stationnaires de type 5.
Enfin, des limites de détection instrumentales très basses ont été atteintes, et se situaient au-dessous de 10 pg pour l’ensemble des composés semi-volatils à l’exception de l’acide benzoïque (14,70 pg) et du 2,4-dinitrophénol (11,53 pg).
Tableau II : Performances d’étalonnage pour l’analyse des composés semi-volatils à l’état de traces sur une colonne RMX-5Sil MS
| Nom du composé | Temps de rétention(min) | Courbe d’étalonnage %RSE | R2 | Point bas (ppb) | Point haut (ppb) | LDI (pg) |
|---|---|---|---|---|---|---|
| N-Nitrosodimethylamine | 3.173 | 16.82 | 5 | 1000 | 2.14 | |
| Pyridine | 3.276 | 8.69 | 0.994 | 10 | 1000 | 3.23 |
| 2-Fluorophenol | 4.532 | 15.24 | 5 | 1000 | 0.28 | |
| Phenol | 5.514 | 19.25 | 1 | 1000 | 0.70 | |
| Phenol-d5 | 5.5 | 17.86 | 1 | 1000 | 0.29 | |
| Aniline | 5.554 | 9.52 | 0.993 | 10 | 1000 | 1.43 |
| Bis(2-chloroethyl) ether | 5.619 | 14.33 | 1 | 1000 | 0.42 | |
| 2-Chlorophenol | 5.688 | 19.78 | 1 | 1000 | 1.28 | |
| 1,3-Dichlorobenzene | 5.863 | 16.96 | 1 | 1000 | 0.36 | |
| 1,4-Dichlorobenzene | 5.944 | 17.90 | 1 | 1000 | 0.77 | |
| Benzyl alcohol | 6.069 | 17.06 | 1 | 1000 | 0.98 | |
| 1,2-Dichlorobenzene | 6.116 | 17.32 | 1 | 1000 | 1.13 | |
| 2-Methylphenol | 6.194 | 19.48 | 10 | 1000 | 1.95 | |
| 2,2′-oxybis(1-chloropropane) | 6.229 | 19.32 | 10 | 1000 | 4.04 | |
| 3- and 4-Methylphenol | 6.369 | 19.71 | 1 | 1000 | 1.01 | |
| N-Nitrosodi-N-propylamine | 6.374 | 5.38 | 0.997 | 10 | 1000 | 3.10 |
| Hexachloroethane | 6.511 | 15.67 | 5 | 1000 | 1.36 | |
| Nitrobenzene | 6.563 | 12.10 | 0.996 | 5 | 1000 | 0.81 |
| Nitrobenzene-d5 | 6.541 | 17.81 | 1 | 1000 | 0.96 | |
| Isophorone | 6.846 | 18.92 | 1 | 1000 | 0.56 | |
| 2-Nitrophenol | 6.941 | 13.56 | 0.996 | 10 | 1000 | 1.26 |
| 2,4-Dimethylphenol | 6.99 | 19.63 | 1 | 1000 | 0.36 | |
| Benzoic acid | 7.019 | 3.84 | 0.998 | 50 | 1000 | 14.70 |
| Bis(2-chloroethoxy)methane | 7.102 | 14.01 | 1 | 1000 | 0.26 | |
| 2,4-Dichlorophenol | 7.223 | 18.99 | 1 | 1000 | 0.83 | |
| 1,2,4-Trichlorobenzene | 7.333 | 10.67 | 1 | 1000 | 0.46 | |
| Naphthalene | 7.424 | 8.68 | 1 | 1000 | 0.73 | |
| 2,6-Dichlorophenol | 7.223 | 18.18 | 1 | 1000 | 0.62 | |
| 4-Chloroaniline | 7.484 | 13.85 | 0.998 | 5 | 1000 | 1.34 |
| Hexachlorobutadiene | 7.59 | 13.96 | 1 | 1000 | 0.65 | |
| 4-Chloro-3-methylphenol | 8.072 | 16.99 | 1 | 1000 | 0.30 | |
| 2-Methylnaphthalene | 8.268 | 10.57 | 1 | 1000 | 0.63 | |
| 1-Methylnaphthalene | 8.388 | 18.50 | 1 | 1000 | 0.64 | |
| Hexachlorocyclopentadiene | 8.474 | 16.59 | 0.998 | 5 | 1000 | 2.72 |
| 2,4,6-Trichlorophenol | 8.613 | 16.69 | 5 | 1000 | 1.55 | |
| 2,4,5-Trichlorophenol | 8.651 | 16.98 | 5 | 1000 | 0.76 | |
| 2-Fluorobiphenyl | 8.721 | 16.31 | 1 | 1000 | 1.05 | |
| 2-Chloronaphthalene | 8.862 | 14.23 | 1 | 1000 | 0.43 | |
| 2-Nitroaniline | 8.979 | 17.82 | 0.996 | 10 | 1000 | 1.33 |
| 1,4-Dinitrobenzene | 9.143 | 12.76 | 0.996 | 10 | 1000 | 8.63 |
| Dimethylphthalate | 9.216 | 18.60 | 1 | 1000 | 0.60 | |
| 1,3-Dinitrobenzene | 9.14 | 18.88 | 0.991 | 10 | 1000 | 6.97 |
| 2,6-Dinitrotoluene | 9.281 | 19.86 | 0.997 | 5 | 1000 | 2.06 |
| Acenapthylene | 9.374 | 11.73 | 1 | 1000 | 0.37 | |
| 3-Nitroaniline | 9.484 | 18.30 | 0.995 | 10 | 1000 | 2.89 |
| Acenaphthene | 9.592 | 9.44 | 0.991 | 1 | 1000 | 2.61 |
| 2,4-Dinitrophenol | 9.617 | 7.79 | 0.995 | 10 | 1000 | 11.53 |
| 4-Nitrophenol | 9.689 | 14.01 | 0.998 | 10 | 1000 | 4.39 |
| 2,4-Dinitrotoluene | 9.778 | 14.84 | 0.999 | 10 | 1000 | 4.30 |
| Dibenzofuran | 9.805 | 9.94 | 1 | 1000 | 0.38 | |
| 2,3,5,6-Tetrachlorophenol | 9.904 | 16.86 | 5 | 1000 | 2.37 | |
| 2,3,4,6-Tetrachlorophenol | 9.958 | 17.72 | 0.997 | 5 | 1000 | 1.74 |
| Diethylphthalate | 10.093 | 15.97 | 1 | 1000 | 0.67 | |
| 4-Chlorophenyl phenyl ether | 10.234 | 7.21 | 1 | 1000 | 0.57 | |
| Fluorene | 10.23 | 14.54 | 1 | 1000 | 0.37 | |
| 4-Nitroaniline | 10.234 | 18.81 | 0.993 | 10 | 1000 | 2.33 |
| 4,6-Dinitro-2-methylphenol | 10.283 | 19.99 | 0.996 | 10 | 1000 | 7.99 |
| N-Nitrosodiphenylamine | 10.376 | 18.03 | 1 | 1000 | 0.53 | |
| Diphenylamine | 10.376 | 18.03 | 1 | 1000 | 0.53 | |
| Diphenylhydrazine | 10.429 | 14.83 | 10 | 1000 | 3.39 | |
| 2,4,6-Tribromophenol | 10.524 | 18.55 | 0.997 | 5 | 1000 | 4.15 |
| 4-Bromophenyl phenyl ether | 10.839 | 15.84 | 1 | 1000 | 0.74 | |
| Hexachlorobenzene | 10.922 | 12.99 | 1 | 1000 | 0.96 | |
| Pentachlorophenol | 11.159 | 16.75 | 0.997 | 5 | 1000 | 1.14 |
| Phenanthrene | 11.421 | 13.06 | 1 | 1000 | 0.18 | |
| Anthracene | 11.484 | 15.30 | 1 | 1000 | 0.92 | |
| Carbazole | 11.68 | 14.68 | 1 | 1000 | 0.52 | |
| Di-n-butylphthalate | 12.131 | 15.80 | 5 | 1000 | 0.25 | |
| Fluoranthene | 12.9 | 10.80 | 1 | 1000 | 0.26 | |
| Benzidine | 13.062 | 19.24 | 0.998 | 10 | 1000 | 1.43 |
| Pyrene | 13.18 | 10.13 | 1 | 1000 | 0.54 | |
| o-Terphenyl-D14 | 13.377 | 13.45 | 1 | 1000 | 0.62 | |
| Butylbenzylphthalate | 14.012 | 15.67 | 5 | 1000 | 0.76 | |
| Bis(2-ethylhexyl)adipate | 14.129 | 18.95 | 0.994 | 10 | 1000 | 1.15 |
| 3’3-Dichlorobenzidine | 14.769 | 17.70 | 0.996 | 10 | 1000 | 1.76 |
| Benz[a]anthracene | 14.805 | 11.61 | 1 | 1000 | 0.38 | |
| Bis(2-ethylhexyl)phthalate | 14.875 | 19.67 | 5 | 1000 | 0.58 | |
| Chrysene | 14.861 | 8.91 | 1 | 1000 | 0.34 | |
| Di-n-octylphthalate | 16 | 18.78 | 0.998 | 5 | 1000 | 0.49 |
| Benzo[b]fluoranthene | 16.691 | 11.15 | 1 | 1000 | 0.41 | |
| Benzo[k]fluoranthene | 16.746 | 13.09 | 1 | 1000 | 0.50 | |
| Benzo[a]pyrene | 17.338 | 12.32 | 1 | 1000 | 0.24 | |
| Dibenz[a,j]acridine | 19.26 | 19.92 | 1 | 1000 | 0.60 | |
| Indeno[1,2,3-cd]pyrene | 19.754 | 15.17 | 1 | 1000 | 0.71 | |
| Dibenz[a,h]anthracene | 19.813 | 13.06 | 1 | 1000 | 0.56 | |
| Benzo[g,h,i]perylene | 20.339 | 10.79 | 1 | 1000 | 0.50 |
Conclusion
Cette étude a confirmé que les colonnes RMX-5Sil MS étaient adéquates pour l’analyse des composés semi-volatils à l’état de traces (moins d’une dizaine de ppb) par GC-MS/MS. La colonne a montré une inertie vis-à-vis d’une grande variété de compositions chimiques (acides, bases, et composés neutres) et a généré d’excellentes courbes d’étalonnages linéaires. La forme et la symétrie des pics sont restées intactes, même à des faibles concentrations auxquelles les composés actifs sont particulièrement difficiles à analyser. La plupart des composés (98 %) ont atteint des limites de détection instrumentales (IDLs) inférieures à 10pg, des gammes d’étalonnage de 1, 5 ou 10 ppb à 1000 ppb et des courbes d’étalonnage présentant un écart-type relatif ≤ 20 %.
Références
- U.S. Environmental Protection Agency, Method 8270E, Semivolatile organic compounds by gas chromatography/mass spectrometry, June 2018. https://www.epa.gov/sites/default/files/2020-10/documents/method_8270e_update_vi_06-2018_0.pdf
- U.S. Environmental Protection Agency, Method 3511 (SW-846), Organic compounds in water by microextraction, July 2014. https://www.epa.gov/hw-sw846/sw-846-test-method-3511-organic-compounds-water-microextraction