Key Highlights
- TriMax不活性化処理により、極めて不活性なサンプルフローパスを実現しました。
- 高い不活性度によりピーク形状が改善され、幅広い半揮発性有機化合物において、ピコグラムレベル以下(サブピコグラム)の装置検出限界(IDL)を達成しました。
- すべての半揮発性有機化合物について、検量線のデータ品質目標である相対標準誤差(%RSE)≤20%を満たしました。検量線下限は安息香酸(50ppb)を除き、すべての化合物で1–10 ppbでした。
Abstract|TriMax不活性化処理による包括的性能検証
本アプリケーションノートでは、RMX-5Sil MSカラムを用いた微量レベルでの半揮発性有機化合物(SVOC)のGC-MS/MS分析性能を評価しました。
その結果、安息香酸(14.70 pg)および2,4-ジニトロフェノール(11.53 pg)を除くすべての化合物において、単一またはサブピコグラムレベルの装置検出限界(IDL)を達成しました。
検量線の相対標準誤差(%RSE)はすべての化合物で20%以下であり、検量線範囲は、安息香酸を除き、1–1000 ppb または 10–1000ppb でした。安息香酸については、50–1000 ppbの範囲で評価しました。
Introduction|SVOC微量分析に求められる不活性度
半揮発性有機化合物(SVOC)は環境中に広く存在し、人の健康への影響が懸念されることから、世界各地でモニタリングが行われています。これらの化合物の分析には、EPA Method 8270Eに代表されるGC-MSやGC-MS/MS法が一般的に用いられています。近年、MS/MS検出器の高い選択性を活用することで、より高感度な分析が可能となり、EPA Method 3511に示されるようなマイクロ抽出法の導入が進んでいます。マイクロ抽出法は、従来法と比較して試料調製時間を短縮できるとともに、最大で1 Lにも及ぶ試料量を必要とする従来の前処理法と比べて、溶媒使用量を大幅に削減できる利点があります。
MS/MS検出の感度を最大限に活かすためには、分析カラムが十分に不活性であり、ピークのS/N比を最大化できることが不可欠です。酸性・塩基性・中性など、化学特性の異なる幅広い半揮発性有機化合物は、カラム表面に存在する活性部位と異なる機構で相互作用するため、包括的に有効な不活性化処理が求められます。
本研究では、微量レベルの半揮発性有機化合物を対象に、RMX-5Sil MSカラムの分析性能を評価しました。特に、分析が困難とされる化合物を含め、広範な化合物群に対するクロマトグラフィー性能および検量線特性を評価し、ピコグラムレベルでの検出が可能であるかを検証しました。
Experimental|評価方法
Standard Preparation|標準溶液およびサンプル調製
検量線作成に用いた混合標準溶液は、市販の標準品を用い、ジクロロメタン中で 1–1000 ppbの濃度範囲(11 濃度点)で調製しました。
Instrument Conditions|分析条件
試料は、RMX-5Sil MS カラム(30 m × 0.25 mm ID × 0.25 µm、cat.# 17323)を用いて測定しました。GC-MS/MS装置には、Shimadzu Nexis GC-2030ガスクロマトグラフと、EIイオン源および高効率コリジョンセルUFsweeperを搭載したShimadzu GCMS-TQ8050 NX超高速質量分析計を使用しました。測定条件は以下のとおりです。
Table I: 微量半揮発性有機化合物分析におけるGC-MS/MS測定条件
| Gas Chromatograph | Shimadzu Nexis GC-2030 |
|---|---|
| FlowColumn | RMX-5Sil MS, 30 m x 0.25 mm ID x 0.25 µm ( cat.# 17323 ) |
| Flow mode | 一定線速度 (39.5 cm/s) |
| Injector mode | スプリット (5:1) |
| Injector liner | 3.5 mm Topaz シングルテーパーライナー, ウール入り ( cat.# 23336 ) |
| Injection volume | 1 µL |
| Injector temperature | 275 °C |
| Oven program | 40 °C (hold 1.5 min) to 280 °C at 20 °C /min to 320 °C at 5 °C /min (hold 1 min) |
| MS system | Shimadzu GCMS-TQ8050 NX ultra-fast mass spectrometer with EI source and UFsweeper high-efficiency collision cell |
| Ionization | 電子衝撃イオン化 (EI) |
| Ionization energy | 70 eV |
| Emission current | 60 mA |
| Acquisition mode | MRM |
| Collision gas | Argon |
| Source temperature | 230 °C |
| GC interface temperature | 300 °C |
Results and Discussion|結果および考察
Chromatographic Performance|難しいSVOC分析で示す優れたピーク性能
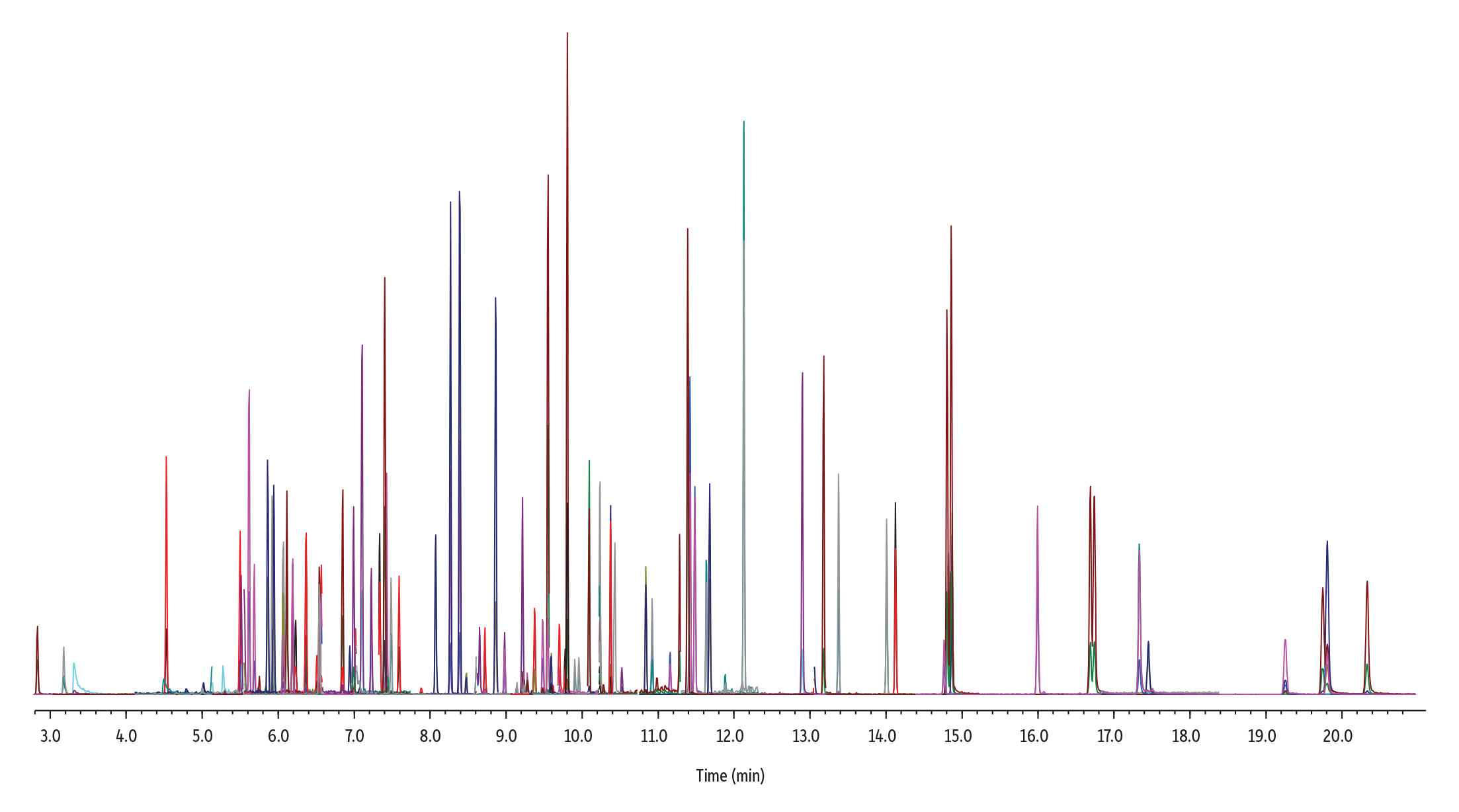
RMX-5Sil MS カラムを用いた GC-MS/MS分析では、50 ppbにおいて86成分の半揮発性有機化合物に対し、良好なピーク形状および分離が得られました。最終溶出成分は21分未満で溶出し、クロマトグラフィー全体にわたって安定した分離が確認されました(Figure 1)。
カラムの不活性度を評価するため、特に問題となりやすい酸性化合物および塩基性化合物について、検量線の低濃度側および高濃度側におけるピークテーリングを評価しました。Figure 2に示すように、高度に不活性化されたカラム表面により、低濃度域においても表面活性の影響が最小限に抑えられ、分析が難しい化合物であっても、積分が容易な対称性の高いピークが得られました。
さらに、この不活性表面処理は固定相の選択性に悪影響を与えることはなく、1 ppbにおいても、多環芳香族炭化水素(PAH)の近接溶出ペアであるbenzo[b]fluorantheneとbenzo[k]fluorantheneが良好に分離されることが確認されました。
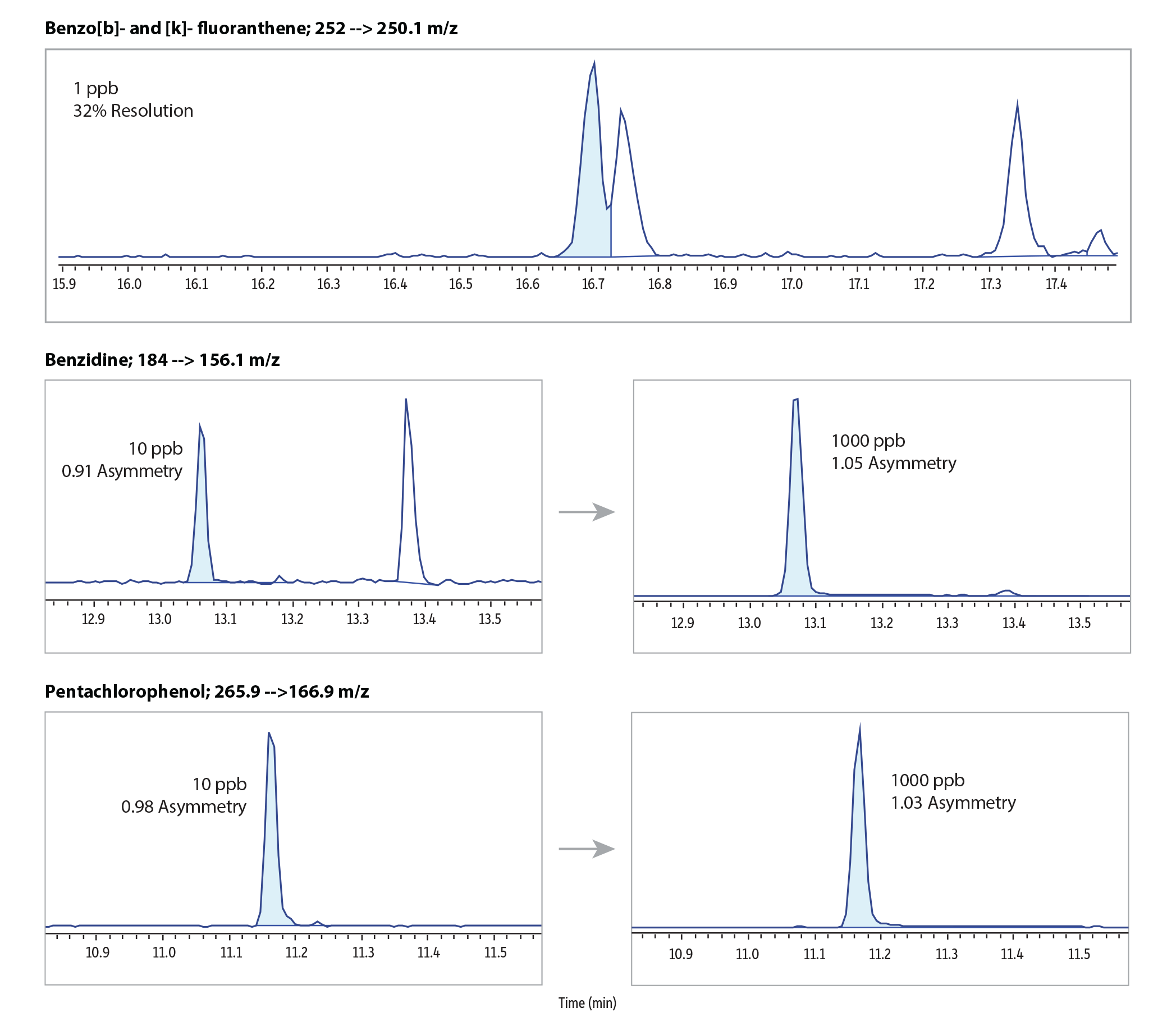
GC_EV1535
Peaks
| Peaks | tR (min) | Transition 1 | Collision energy 1 | Transition 2 | Collision energy 2 | |
|---|---|---|---|---|---|---|
| 1. | Benzidine | 13.062 | 184.00>156.10 | 24 | 184.00>167.10 | 24 |
| 2. | Benzo[b]fluoranthene | 16.691 | 252.10>250.10 | 36 | 250.10>248.10 | 36 |
| 3. | Benzo[k]fluoranthene | 16.746 | 252.10>250.10 | 36 | 250.10>248.10 | 36 |
| 4. | Pentachlorophenol | 11.159 | 265.90>164.90 | 26 | 265.90>166.90 | 26 |
Calibration Performance|低濃度域まで安定した検量線
Table IIに示すように、Shimadzu GC-MS/MSシステムと、高度に不活性化されたRMX-5Sil MS分析カラムの組み合わせにより、幅広い半揮発性有機化合物クラスにおいて、優れた微量レベルの分析感度が得られました。検量線の相対標準誤差(%RSE)は、すべての化合物で20%以下であり、検量線に関するデータ品質目標を満たしました。また、代表的な半揮発性機化合物の一部について決定係数(R²)を評価した結果、評価対象となったすべての化合物でR² ≥ 0.99が得られました。すべての半揮発性有機化合物において、検量線範囲は1–000 ppbまたは10–1000 ppbであり、安息香酸のみ50–1000ppbでした。安息香酸について直線範囲の下限がやや高くなった点は、5系固定相に対する溶解性が低いことから、想定内の結果と考えられます。さらに、装置検出限界(IDL)は、安息香酸(14.70 pg)および2,4-ジニトロフェノール(11.53 pg)を除き、すべての半揮発性有機化合物でピコグラムレベル以下(サブピコグラム)を達成しました。
Table II: RMX-5Sil MSカラムを用いた微量半揮発性有機化合物分析における検量線評価
| Compound Name | Retention Time (min) | Calibration Curve %RSE | R2 | Low Point (ppb) | High Point (ppb) | IDL (pg) |
|---|---|---|---|---|---|---|
| N-Nitrosodimethylamine | 3.173 | 16.82 | 5 | 1000 | 2.14 | |
| Pyridine | 3.276 | 8.69 | 0.994 | 10 | 1000 | 3.23 |
| 2-Fluorophenol | 4.532 | 15.24 | 5 | 1000 | 0.28 | |
| Phenol | 5.514 | 19.25 | 1 | 1000 | 0.70 | |
| Phenol-d5 | 5.5 | 17.86 | 1 | 1000 | 0.29 | |
| Aniline | 5.554 | 9.52 | 0.993 | 10 | 1000 | 1.43 |
| Bis(2-chloroethyl) ether | 5.619 | 14.33 | 1 | 1000 | 0.42 | |
| 2-Chlorophenol | 5.688 | 19.78 | 1 | 1000 | 1.28 | |
| 1,3-Dichlorobenzene | 5.863 | 16.96 | 1 | 1000 | 0.36 | |
| 1,4-Dichlorobenzene | 5.944 | 17.90 | 1 | 1000 | 0.77 | |
| Benzyl alcohol | 6.069 | 17.06 | 1 | 1000 | 0.98 | |
| 1,2-Dichlorobenzene | 6.116 | 17.32 | 1 | 1000 | 1.13 | |
| 2-Methylphenol | 6.194 | 19.48 | 10 | 1000 | 1.95 | |
| 2,2′-oxybis(1-chloropropane) | 6.229 | 19.32 | 10 | 1000 | 4.04 | |
| 3- and 4-Methylphenol | 6.369 | 19.71 | 1 | 1000 | 1.01 | |
| N-Nitrosodi-N-propylamine | 6.374 | 5.38 | 0.997 | 10 | 1000 | 3.10 |
| Hexachloroethane | 6.511 | 15.67 | 5 | 1000 | 1.36 | |
| Nitrobenzene | 6.563 | 12.10 | 0.996 | 5 | 1000 | 0.81 |
| Nitrobenzene-d5 | 6.541 | 17.81 | 1 | 1000 | 0.96 | |
| Isophorone | 6.846 | 18.92 | 1 | 1000 | 0.56 | |
| 2-Nitrophenol | 6.941 | 13.56 | 0.996 | 10 | 1000 | 1.26 |
| 2,4-Dimethylphenol | 6.99 | 19.63 | 1 | 1000 | 0.36 | |
| Benzoic acid | 7.019 | 3.84 | 0.998 | 50 | 1000 | 14.70 |
| Bis(2-chloroethoxy)methane | 7.102 | 14.01 | 1 | 1000 | 0.26 | |
| 2,4-Dichlorophenol | 7.223 | 18.99 | 1 | 1000 | 0.83 | |
| 1,2,4-Trichlorobenzene | 7.333 | 10.67 | 1 | 1000 | 0.46 | |
| Naphthalene | 7.424 | 8.68 | 1 | 1000 | 0.73 | |
| 2,6-Dichlorophenol | 7.223 | 18.18 | 1 | 1000 | 0.62 | |
| 4-Chloroaniline | 7.484 | 13.85 | 0.998 | 5 | 1000 | 1.34 |
| Hexachlorobutadiene | 7.59 | 13.96 | 1 | 1000 | 0.65 | |
| 4-Chloro-3-methylphenol | 8.072 | 16.99 | 1 | 1000 | 0.30 | |
| 2-Methylnaphthalene | 8.268 | 10.57 | 1 | 1000 | 0.63 | |
| 1-Methylnaphthalene | 8.388 | 18.50 | 1 | 1000 | 0.64 | |
| Hexachlorocyclopentadiene | 8.474 | 16.59 | 0.998 | 5 | 1000 | 2.72 |
| 2,4,6-Trichlorophenol | 8.613 | 16.69 | 5 | 1000 | 1.55 | |
| 2,4,5-Trichlorophenol | 8.651 | 16.98 | 5 | 1000 | 0.76 | |
| 2-Fluorobiphenyl | 8.721 | 16.31 | 1 | 1000 | 1.05 | |
| 2-Chloronaphthalene | 8.862 | 14.23 | 1 | 1000 | 0.43 | |
| 2-Nitroaniline | 8.979 | 17.82 | 0.996 | 10 | 1000 | 1.33 |
| 1,4-Dinitrobenzene | 9.143 | 12.76 | 0.996 | 10 | 1000 | 8.63 |
| Dimethylphthalate | 9.216 | 18.60 | 1 | 1000 | 0.60 | |
| 1,3-Dinitrobenzene | 9.14 | 18.88 | 0.991 | 10 | 1000 | 6.97 |
| 2,6-Dinitrotoluene | 9.281 | 19.86 | 0.997 | 5 | 1000 | 2.06 |
| Acenapthylene | 9.374 | 11.73 | 1 | 1000 | 0.37 | |
| 3-Nitroaniline | 9.484 | 18.30 | 0.995 | 10 | 1000 | 2.89 |
| Acenaphthene | 9.592 | 9.44 | 0.991 | 1 | 1000 | 2.61 |
| 2,4-Dinitrophenol | 9.617 | 7.79 | 0.995 | 10 | 1000 | 11.53 |
| 4-Nitrophenol | 9.689 | 14.01 | 0.998 | 10 | 1000 | 4.39 |
| 2,4-Dinitrotoluene | 9.778 | 14.84 | 0.999 | 10 | 1000 | 4.30 |
| Dibenzofuran | 9.805 | 9.94 | 1 | 1000 | 0.38 | |
| 2,3,5,6-Tetrachlorophenol | 9.904 | 16.86 | 5 | 1000 | 2.37 | |
| 2,3,4,6-Tetrachlorophenol | 9.958 | 17.72 | 0.997 | 5 | 1000 | 1.74 |
| Diethylphthalate | 10.093 | 15.97 | 1 | 1000 | 0.67 | |
| 4-Chlorophenyl phenyl ether | 10.234 | 7.21 | 1 | 1000 | 0.57 | |
| Fluorene | 10.23 | 14.54 | 1 | 1000 | 0.37 | |
| 4-Nitroaniline | 10.234 | 18.81 | 0.993 | 10 | 1000 | 2.33 |
| 4,6-Dinitro-2-methylphenol | 10.283 | 19.99 | 0.996 | 10 | 1000 | 7.99 |
| N-Nitrosodiphenylamine | 10.376 | 18.03 | 1 | 1000 | 0.53 | |
| Diphenylamine | 10.376 | 18.03 | 1 | 1000 | 0.53 | |
| Diphenylhydrazine | 10.429 | 14.83 | 10 | 1000 | 3.39 | |
| 2,4,6-Tribromophenol | 10.524 | 18.55 | 0.997 | 5 | 1000 | 4.15 |
| 4-Bromophenyl phenyl ether | 10.839 | 15.84 | 1 | 1000 | 0.74 | |
| Hexachlorobenzene | 10.922 | 12.99 | 1 | 1000 | 0.96 | |
| Pentachlorophenol | 11.159 | 16.75 | 0.997 | 5 | 1000 | 1.14 |
| Phenanthrene | 11.421 | 13.06 | 1 | 1000 | 0.18 | |
| Anthracene | 11.484 | 15.30 | 1 | 1000 | 0.92 | |
| Carbazole | 11.68 | 14.68 | 1 | 1000 | 0.52 | |
| Di-n-butylphthalate | 12.131 | 15.80 | 5 | 1000 | 0.25 | |
| Fluoranthene | 12.9 | 10.80 | 1 | 1000 | 0.26 | |
| Benzidine | 13.062 | 19.24 | 0.998 | 10 | 1000 | 1.43 |
| Pyrene | 13.18 | 10.13 | 1 | 1000 | 0.54 | |
| o-Terphenyl-D14 | 13.377 | 13.45 | 1 | 1000 | 0.62 | |
| Butylbenzylphthalate | 14.012 | 15.67 | 5 | 1000 | 0.76 | |
| Bis(2-ethylhexyl)adipate | 14.129 | 18.95 | 0.994 | 10 | 1000 | 1.15 |
| 3’3-Dichlorobenzidine | 14.769 | 17.70 | 0.996 | 10 | 1000 | 1.76 |
| Benz[a]anthracene | 14.805 | 11.61 | 1 | 1000 | 0.38 | |
| Bis(2-ethylhexyl)phthalate | 14.875 | 19.67 | 5 | 1000 | 0.58 | |
| Chrysene | 14.861 | 8.91 | 1 | 1000 | 0.34 | |
| Di-n-octylphthalate | 16 | 18.78 | 0.998 | 5 | 1000 | 0.49 |
| Benzo[b]fluoranthene | 16.691 | 11.15 | 1 | 1000 | 0.41 | |
| Benzo[k]fluoranthene | 16.746 | 13.09 | 1 | 1000 | 0.50 | |
| Benzo[a]pyrene | 17.338 | 12.32 | 1 | 1000 | 0.24 | |
| Dibenz[a,j]acridine | 19.26 | 19.92 | 1 | 1000 | 0.60 | |
| Indeno[1,2,3-cd]pyrene | 19.754 | 15.17 | 1 | 1000 | 0.71 | |
| Dibenz[a,h]anthracene | 19.813 | 13.06 | 1 | 1000 | 0.56 | |
| Benzo[g,h,i]perylene | 20.339 | 10.79 | 1 | 1000 | 0.50 |
Conclusion|単一メソッド化を可能にする高不活性カラム
本研究により、RMX-5Sil MSカラムが、GC-MS/MSを用いた微量レベル(1桁 ppb)の半揮発性有機化合物分析に適していることが確認されました。RMX-5Sil MSカラムは、酸性・塩基性・中性といった幅広い化学特性をもつ化合物に対して高い不活性度を示し、優れた検量線直線性を実現しました。特に、活性化合物の分析が困難となる低濃度域においても、ピーク形状および対称性は良好に維持されました。
評価対象化合物のうち、98% がピコグラムレベル以下(サブピコグラム)の装置検出限界を達成し、検量線範囲は 1、5、または10 ppbから1000 ppbで設定可能でした。また、すべての検量線において相対標準誤差(%RSE)20%以下を満たしました。
References
- U.S. Environmental Protection Agency, Method 8270E, Semivolatile organic compounds by gas chromatography/mass spectrometry, June 2018. https://www.epa.gov/sites/default/files/2020-10/documents/method_8270e_update_vi_06-2018_0.pdf
- U.S. Environmental Protection Agency, Method 3511 (SW-846), Organic compounds in water by microextraction, July 2014. EPA Method 3511 (SW-846): Organic Compounds in Water by Microextraction | US EPA